Warren Chan最新研究:流速会不会影响纳米摄取?
 NanoLabs
NanoLabs
2020-05-12


纳米颗粒通常通过全身注射来给药,这使得它们暴露于血流的动态环境中。注射的纳米颗粒在血液中以各种流速传播,这些流速会引起不同的血管剪切速率。内皮细胞在这些血管中排列,在循环过程中摄取纳米颗粒,但是这种相互作用在体内的流量依赖性却很难表征。
有鉴于此,加拿大多伦多大学陈志和(Warren C. W. Chan)教授课题组开发了一种微流控系统来控制纳米颗粒与内皮细胞相互作用时的流速,探索流速对“纳米粒子-细胞”相互作用的影响。
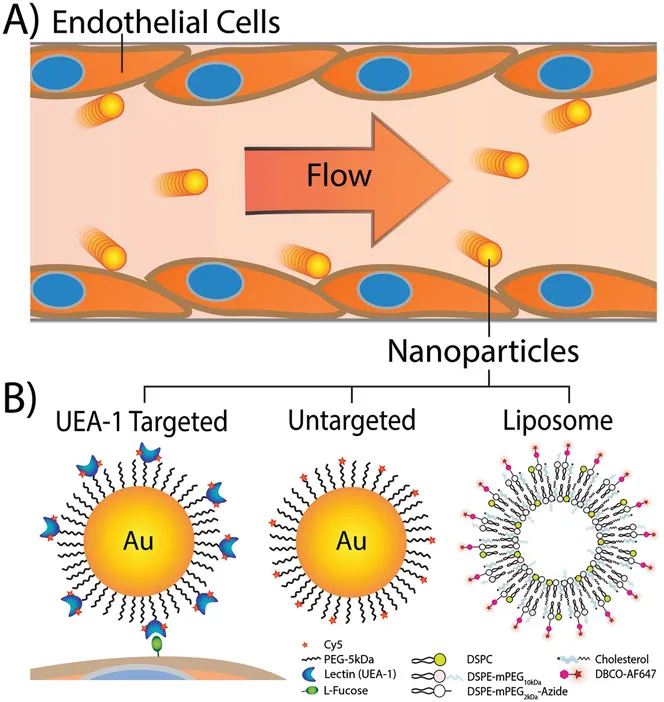

图 | 流动下的纳米颗粒-内皮细胞相互作用。
实验装置
首先我们来看看,作者是怎么控制流速的,如下图所示,整个实验装置由蠕动泵(peristaltic pump)、微流芯片(Microfluidic chip)和培养液储存器组成。使用微流体技术能够控制流体流速和内皮细胞暴露于纳米颗粒时所经历的剪切应力。

装置图


图 | 内皮细胞装置的制备
流速与细胞摄取成反比
研究人员将纳米金颗粒在内皮细胞中的摄取以不同的流速进行定量,发现流速的增加会导致纳米颗粒的摄取减少。内皮细胞对增加的流量剪切速率响应,使得吸收纳米颗粒的能力降低。该平台能够显示流速对细胞与纳米颗粒之间相互作用的影响:流速与细胞摄取之间存在反比关系。

剪切力改变与细胞摄取
靶向化是否有影响?
研究人员还发现,使用靶向剂结合内皮细胞可以减轻血流速度的某些影响。用内皮细胞结合配体修饰纳米颗粒表面可以将吸收部分地恢复到非流动水平,这表明功能化纳米颗粒结合内皮细胞可以使纳米颗粒抵抗流动效应。

图 | 纳米颗粒流速的增加会减少摄取。
小结:
综上,该项工作是第一代旨在探索流速对“纳米粒子-细胞”相互作用影响的微流控系统,设计简单。但体内的血管情况更为复杂,未来的微流体系统将需要包括更复杂的微流控结构来模仿这种曲折的脉管系统,需要开发这样的装置来对纳米颗粒与生物系统之间的相互作用进行基础研究。这些研究对于设计用于医疗应用的纳米材料至关重要。
参考文献:
Yih Yang Chen et al. Flow Rate Affects Nanoparticle Uptake into Endothelial Cells. Adv. Mater. 2020.
https://doi.org/10.1002/adma.201906274
关于陈志和教授的近期相关文章可参考:
1. Nature Materials:挑战传统! 临床30年后,肿瘤纳米给药机制新发现!
2. 3篇Nature Materials齐报道:聂书明等人评述主动转胞吞作用和癌症纳米医学的新机遇
3. Warren Chan等JACS:剖析纳米材料上的蛋白冠