颠覆认知!叶酸并不能增强纳米药物靶向性?
 NanoLabs
NanoLabs
2020-11-09
叶酸受体(FR)是介导叶酸及其衍生物内吞的糖基磷脂酰肌醇连接膜糖蛋白。已在人体中鉴定出两种膜结合的FR异构体(FR-α和FR-β),均显示出与叶酸的极高结合亲和力并有效促进叶酸的细胞内运输。在许多人类癌症中已经观察到FR-α的表达上调,并且FR-α的高表达水平通常与晚期组织学侵袭性相关。FR-α高表达在人类癌症中使其成为靶向递送的理想候选靶点。在过去的几十年中,为治疗,诊断和手术导航目的而针对FR-α做出了许多努力。不幸的是,目前还没有一种药物被批准用于临床。
究其原因,为何该靶向分子在临床表现不行?
成果简介
鉴于此,复旦大学占昌友教授等人重新研究了血浆蛋白对FA功能化纳米药物体内命运的调节作用,重新探索了叶酸在体内的靶向能力。成果发表于ACS Nano杂志上。
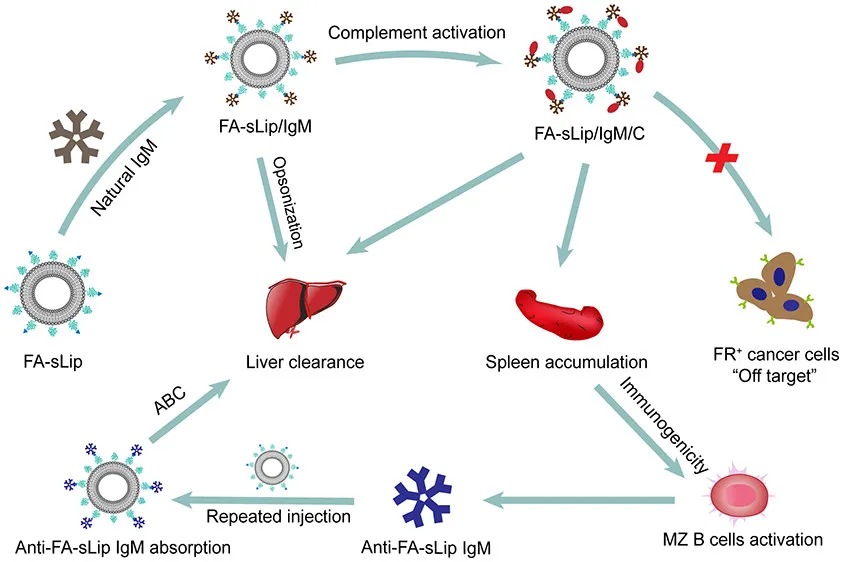

剥夺靶向,还被捕获
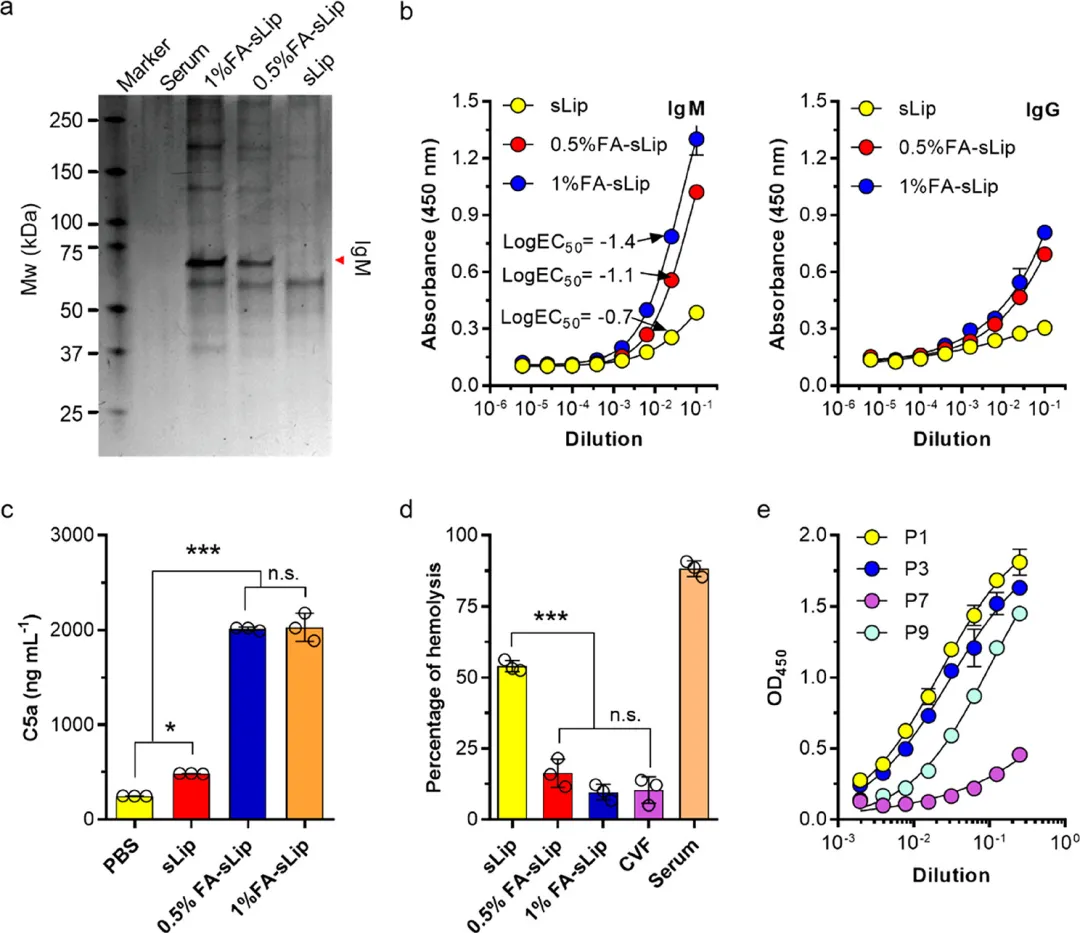
发现FA功能化会诱导脂质体表面被大量天然IgM吸附,这剥夺FA受体识别的能力,加速体内补体激活。与普通脂质体(不含FA)相比,FA功能化并不会增强脂质体在FR-α高表达肿瘤中的分布,反而会加剧巨噬细胞在肿瘤、肝脏和脾脏中对脂质体的捕获。

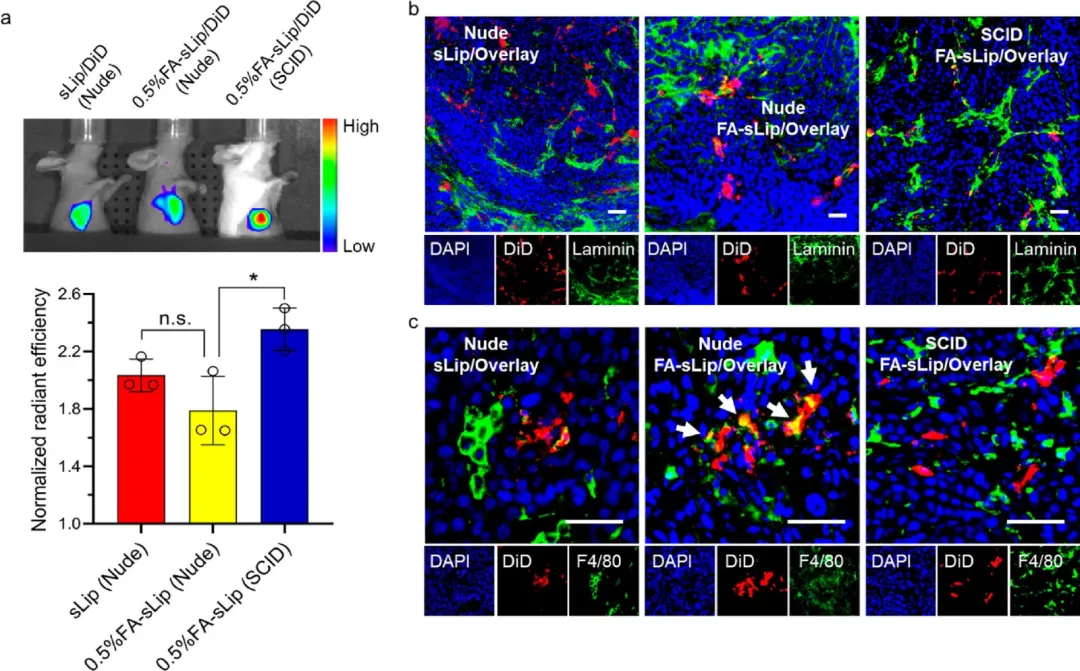
临床应用需谨慎
此外,FA功能化聚合物纳米粒子也容易受到天然IgM吸附的影响。这项工作强调了天然IgM在调节FA功能化纳米药物体内给药中的关键作用。由于免疫紊乱和免疫球蛋白水平与癌症患者的普遍联系,FA靶向给药系统的临床应用需要格外谨慎。

参考文献:
Huan Wang, et al., Interrogation of Folic Acid-Functionalized Nanomedicines: The Regulatory Roles of Plasma Proteins Reexamined. ACS Nano 2020.
DOI: 10.1021/acsnano.0c02821
https://pubs.acs.org/doi/10.1021/acsnano.0c02821