纳米银,勇登Nature Nanotechnology!
 奇物论
奇物论
2021-05-19
银纳米颗粒(AgNPs)由于其抗菌活性已在许多消费品中商业化,在食品包装、生物医药和环境工业中具有潜在的应用前景。尽管AgNPs在消费品中越来越普遍,但AgNPs的生物学作用机制尚不清楚。这种了解的缺乏不仅阻碍了新的治疗性银纳米制剂的开发,而且也妨碍了对非靶细胞和或生物体毒性的准确预测。AgNPs的毒性机制通常归因于离子颗粒表面离子Ag+的释放,暴露于AgNPs的细胞已表现出炎症、氧化、遗传毒性和细胞毒性反应。相反,一些研究提出由AgNPs的物理化学性质驱动的颗粒特异性不良反应是主要机制。这种粒子特异性的作用在很大程度上仍有待研究;诸如NP与细胞表面的相互作用、NP的摄取和细胞内的化学转化等动力学过程尚不清楚。在文献中提出的毒性途径的机制解释中,有一种叫做“特洛伊木马机制”。据推测,NPs起着Ag+载体的作用,因为在细胞外环境中,离子很难避开络合而进入细胞内空间。一旦内化,NPs经历溶酶体增强溶解和释放Ag+,这对细胞功能产生负面影响。因此,确定AgNPs毒性作用的罪魁祸首的关键是:在细胞间和细胞内环境中检测上述离子和粒子。然而,AgNPs的原位鉴定及其表征和定量仍然是一个方法学上的挑战,这不仅是AgNPs的共同挑战,也是NPs的共同挑战。因此,很明显,目前害没有任何一种技术能够提供有关NPs的细胞相互作用和细胞内命运的足够详细的信息。鉴于此,澳大利亚南澳大学Enzo Lombi等人采用一种结合了多种分析技术的方法来阐明AgNPs暴露于人类细胞后的命运,并研究其摄取行为。相关成果发表在Nature Nanotechnology上。

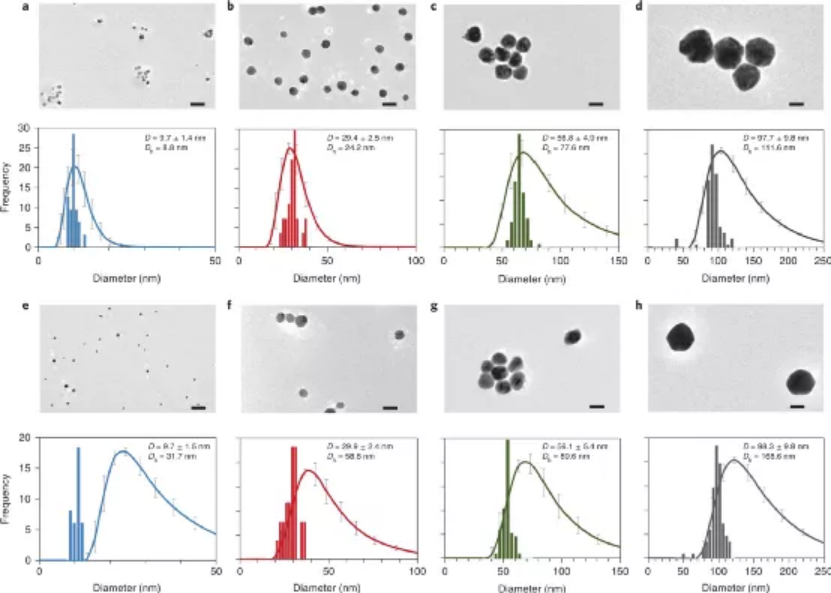
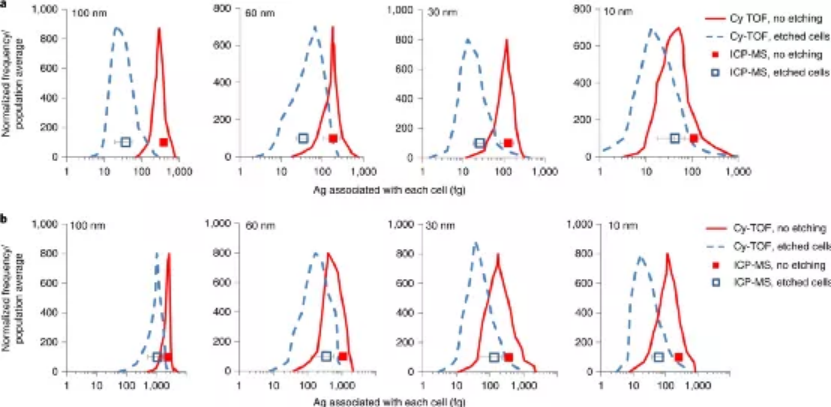
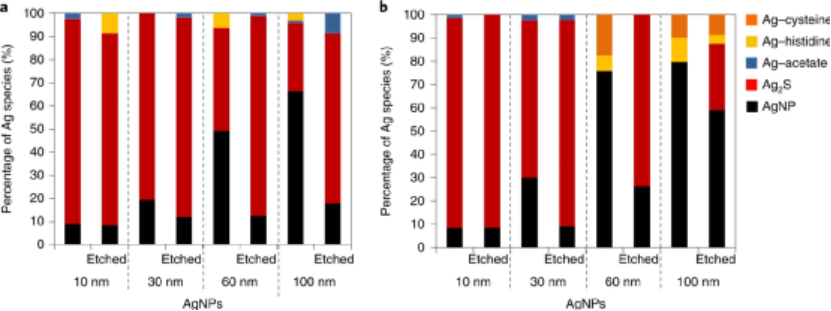
(1)ICP-MS化学分析和质谱流式细胞技术(Cy-TOF)在单个细胞水平上测量与细胞相关的Ag;(2)使用ICP-MS单颗粒检测(sp-ICP-MS)鉴定和表征与细胞相黏附并被细胞内在化的含银NP;(3)同步辐射X射线吸收光谱(XAS)鉴定细胞相关银的化学形态;(4)化学蚀刻以区分与细胞表面结合的Ag与细胞内的Ag。研究人员选择了8种AgNPs配方来研究不同表面电荷和主要NP尺寸(10、30、60、100 nm)引起的不同的NP-细胞相互作用。而且由于人类T淋巴细胞细胞系的丰富性和适应性免疫的相关性,因此选择其作为细胞模型。研究发现,带有阳离子表面电荷(即bPEI包被)的AgNP比具有相同主要尺寸的阴离子(即柠檬酸盐包被的)AgNP具有明显更高的细胞毒性,对于具有相同表面涂层的AgNP,基于质量的毒性随着粒径的减小而增加。而且阳离子纳米颗粒更容易被细胞黏附,而且还表明内在化的Ag在驱动AgNP毒性中起主要作用。为了研究细胞相关和细胞内AgNPs的潜在转化并研究细胞外环境中Ag的形态,通过XANES光谱分析了对AgNP暴露的细胞和暴露介质进行了分析。暴露于AgNPs 24小时后,金属Ag和硫化Ag(Ag2S)是与淋巴细胞相关的Ag的两种主要形式。细胞样品中金属银的含量明显依赖于AgNPs的原始大小。值得注意的是,在未蚀刻的样品中发现了更多的金属Ag,这表明大多数AgNP黏附在细胞膜的外部。而在蚀刻的样品中,与细胞黏附的总Ag含量较低,并且检测到的金属Ag含量较小。这些结果表明,硫化部分显然发生在细胞内。也就是说,AgNPs的生物转化主要受硫化作用的影响,这可以看作是Ag的细胞解毒途径之一。图|AgNP暴露的人T淋巴细胞表面和细胞内Ag的形态总而言之,这项研究提供了一个框架,可通过使用互补的分析方法全面了解NP与哺乳动物细胞之间的相互作用。这项工作强调了联合方法的重要性,如单细胞,单粒子和原位物种形成技术,以解开未知的NP-细胞相互作用。Malysheva, A., Ivask, A., Doolette, C.L. et al. Cellular binding, uptake and biotransformation of silver nanoparticles in human T lymphocytes. Nat. Nanotechnol. (2021).https://doi.org/10.1038/s41565-021-00914-3
 奇物论
奇物论

 奇物论
奇物论



